2024年年底四款抗癌抗肿瘤新药上市在即,狙击肺癌、胰腺癌、乳腺癌、血癌等,完全缓解率超50%
发布日期:2024-11-15 浏览次数:
2024年年底四款抗癌抗肿瘤新药上市在即,狙击肺癌、胰腺癌、乳腺癌、血癌等,完全缓解率超50%
时光荏苒,如白驹过隙,转眼间2024年已步入尾声。在这一年里,抗癌领域喜讯连连,我们不仅迎来了具有里程碑意义的首款获批上市的TCR-T细胞疗法——afami-cel,而且见证了众多抗癌新药、新技术如雨后春笋般相继问世。这些成果宛如一盏盏明灯,为深陷黑暗的癌症患者点亮了生命的新希望,让他们在与病魔的艰苦斗争中看到了曙光。
更令人振奋不已的是,在2024年最后的两个月里,还有多款抗癌新药已蓄势待发!全球肿瘤医生网小编为大家整理汇总了岁末有望获批上市的四大抗癌新药的相关信息,帮广大癌友树立战胜癌症的坚定信心!
四大抗癌新药蓄势待发,2024岁末有望获批上市
Zenocutuzumab
药品信息
●药物名称:Zenocutuzumab(泽妥珠单抗,Zeno)
●治疗靶点:HER2、HER3
●适应证:NRG1阳性非小细胞肺癌(NSCLC)或胰腺癌(PDAC)
药物介绍
Zenocutuzumab(泽妥珠单抗,Zeno,MCLA-128)是由Merus公司研发的一款靶向HER3、HER2的双特异性抗体,美国食品药品监督管理局(FDA)已对Zenocutuzumab的生物制品许可申请 (BLA) 给予优先审查,用于治疗NRG1(神经调节蛋白1融合)阳性非小细胞肺癌(NSCLC)或胰腺癌(PDAC),预计将审查时间从10个月缩短至6个月。
如果能顺利获批,Zenocutuzumab将成为NRG1阳性肺癌和胰腺癌患者的首个也是唯一一个靶向疗法!而且与目前可用疗法相比,或将有显著改善,为NRG1阳性患者提供了重要的潜在治疗机会!
肺癌:近80%患者靶病变缩小
Zenocutuzumab治疗肺癌的1/2期eNRGy临床研究(NCT02912949),共入组85例晚期NRG1阳性非小细胞肺癌(NSCLC)患者,年龄≥ 18 岁,既往接受过标准疗法治疗或不适合接受标准疗法治疗,入组接受Zenocutuzumab治疗。
结果显示:根据RECIST v1.1确认的客观缓解率(ORR)达到37.2%(29/78,95% CI 26.5-48.9)(详见下图)。其中,78%的患者出现靶病变缩小表现。中位缓解持续时间(DOR)长达12.9个月,6个月DOR率高达79%。

▲图源“ESMO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
胰腺癌:客观缓解率超40%
Zenocutuzumab治疗肺癌的1/2期eNRGy临床研究(NCT02912949),共入组85例晚期NRG1阳性非小细胞肺癌(NSCLC)患者,年龄≥ 18 岁,既往接受过标准疗法治疗或不适合接受标准疗法治疗,入组接受Zenocutuzumab治疗。结果显示:
2023 ESMO大会上报道了Zenocutuzumab治疗胰腺癌的研既往究结果,共入组38例中位年龄为 49 岁(范围 21-72)的晚期 NRG1阳性的胰腺癌(PDAC)患者。
结果显示:确认的客观缓解率(ORR)达到44%(95%CI26-65),其中1例患者幸运地获得了完全缓解(CR)、11例达到部分缓解(PR)。81%的患者靶病变缩小,中位缓解持续时间(DOR)达9.1个月(详见下图),6个月DOR率为64%。
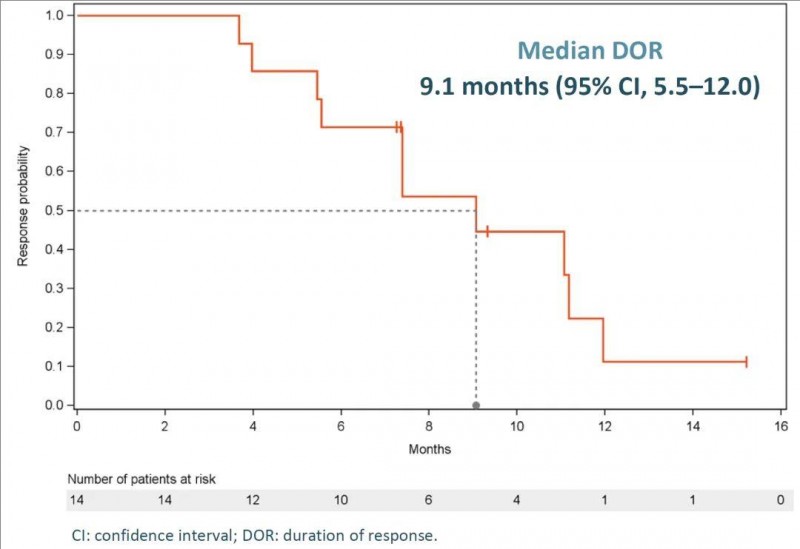
▲图源“ESMO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
Zenocutuzumab
药品信息
●药物名称:Zanidatamab(泽尼达妥单抗、ZW 25)
●治疗靶点:HER2
●适应证:不可切除的、局部晚期或转移性HER2阳性胆道癌(BTC)
药物介绍
Zanidatamab是一款针对人类表皮生长因子受体2(HER2)的双特异性抗体,用于治疗先前接受过治疗的、不可切除的、局部晚期或转移性HER2阳性胆道癌(BTC)。2024年5月29日,被美国FDA授予优先审查资格,如果能顺利获批,该药将成为首个获FDA批准用于治疗HER2阳性局部晚期或转移性胆道癌的HER2靶向药。
临床研究数据
Zanidatamab的生物制品许可申请(BLA),主要是基于2b期HERIZON-BTC-01临床试验(NCT04466891)的惊艳结果。本次研究共入组87例局部晚期不可切除或转移性胆道癌(BTC)患者[包括胆囊癌(GBC)、肝内/肝外胆管癌(ICC/ECC)],入组接受Zanidatamab治疗。
结果显示:在队列1(n=80)中,客观缓解率(ORR)达到41%(详见下表),中位缓解持续时间(DOR)长达12.9个月。在数据截止时(2022年10月10日)的33例应答者中,49%持续缓解,82%的DOR≥16周。
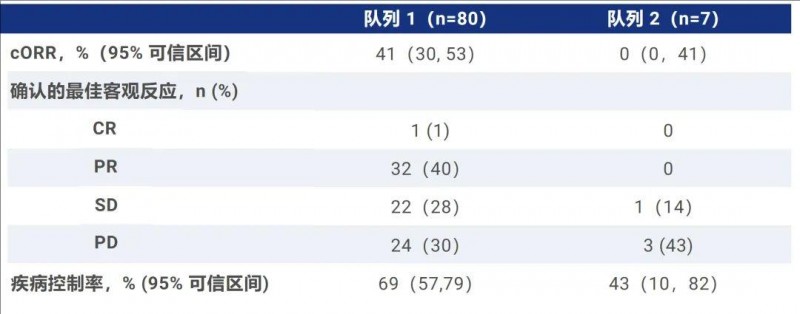
▲数据源自“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
芦康沙妥珠单抗
药品信息
●药物名称:芦康沙妥珠单抗(Sacituzumab Govitecan,SG,Trodelvy)
●治疗靶点:TROP2
●适应证:非小细胞肺癌、乳腺癌、尿路上皮癌
药物介绍
芦康沙妥珠单抗(Sacituzumab Govitecan,SG,Trodelvy)是我国科伦博泰自主研发的一款TROP2(滋养层细胞表面抗原 2)抗体偶联药物(ADC),已在美国和其他多个国家获批,用于治疗转移性乳腺癌、三阴性乳腺癌、化疗和免疫疗法治疗后的转移性尿路上皮癌。
近期,芦康沙妥珠单抗被中国国家药品监督管理局(NMPA)纳入优先审评,用于治疗不可切除的局部晚期或转移性三阴性乳腺癌、局部晚期或转移性EGFR突变非小细胞肺癌。如果能顺利获批上市,该药将成为中国首款原创的治疗肺癌的TROP2新型ADC药物。
临床研究数据
芦康沙妥珠单抗治疗转移性乳腺癌的TROPiCS-02研究(NCT04639986),共入组331例HR+HER2−转移性乳腺癌(mBC)患者,将其分为两组,即SG(n=166,接受芦康沙妥珠单抗治疗)、化疗组(n=165)。
结果显示:与化疗相比,接受芦康沙妥珠单抗治疗的患者中位无进展生存期(PFS)有所改善,分别为4.3个月(SG组) vs 4.2个月(化疗组)。6个月PFS率分别为41%(SG组) vs 24%(化疗组)。疾病进展或死亡风险降低了34%。

▲图源“nature medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
obe-cel
药品信息
●药物名称:obe-cel(obecabtagene autoleucel)
●研发公司:CD19
●适应证:复发/难治性B细胞急性淋巴细胞白血病(R/R B-ALL)
药物介绍
Obe-cel(obecabtagene autoleucel)是一款针对CD19的自体CAR-T细胞产品,其生物制品许可申请(BLA),已被美国FDA受理,用于成人复发/难治性(R/R)B细胞急性淋巴细胞白血病(ALL)的治疗。此前该药已获得欧洲药品管理局(EMA)和美国食品药品监督管理局(FDA)授予的孤儿药资格认定。
临床研究数据
Obe-cel此次提交的BLA申请,主要是基于2023美国临床肿瘤学会(ASCO)年会、2023美国血液学会(ASH)年会上,公布的2期FELIX研究(NCT04404660)的惊艳数据,完全缓解率超50%,达到了惊人的57%!
截至2023年3月16日,共126例B细胞急性淋巴细胞白血病(R/R B-ALL)患者入组并成功接受了obe-cel治疗。经过11.0个月的中位随访,结果显示:CR/CRi(“完全缓解”或“完全缓解但计数不完全恢复”)率高达77%,CR(完全缓解)率达到57%。此外,在可评估MRD(微小残留病灶)反应的患者中,高达96%的患者达到MRD阴性状态。
印度肿瘤药房(India Pharmacy)是印度新德里肿瘤药房信息咨询服务平台,旨在为患者提供各类进口原研 进口仿制 最新研制等医药信息咨询 跨境医药电商直邮服务,让患者轻松获取全球最佳药品有更多选择,基本涵盖新特药 抗癌药 靶向药 丙肝 乙肝 高血压 糖尿病 痛风 等药品,欢迎咨询!官方微信 Yindu7689
- 上一篇:刚刚!武田靶向EGFR-20in的不可逆抑制剂Mobocertinib在中国获批上市
- 下一篇:没有了


