PD-(L)1单抗「大举进军」肺癌新辅助治疗领域,方案究竟怎么选?
发布日期:2021-12-12 浏览次数:次
2021年世界肺癌大会(WCLC)于9月8日-14日举行。会议上公布了多项解读早期肺癌治疗及其预后因素的相关研究结果,让我们一睹为快!
本次WCLC会议上公布了帕博利珠单抗用于早期非小细胞肺癌(NSCLC)新辅助治疗的最终安全性分析、主要研究终点和更新的疗效结果。
研究者发起了 I 期单中心研究,以评估帕博利珠单抗新辅助治疗 I-II 期 (TNM v7) 可切除NSCLC的安全性,确定推荐的 II 期剂量/时间表 (RP2D/S) ,并通过残余存活肿瘤评估疗效(残余存活肿瘤≤10% 定义为主要病理反应,MPR)。
该研究共纳入了26 例患者,没有发生剂量限制毒性(DLT) 和 5 级治疗相关不良反应(TRAE)。2例患者(8%,95% CI 0-18%)发生了3-4 级 TRAE;1例患者同时患有 3 级脑炎和心肌炎(导致手术延期),还有1例患者同时患有 3 级脑炎和肝炎(手术后,分别发生在帕博利珠单抗开始应用后的124 天和 171 天)。
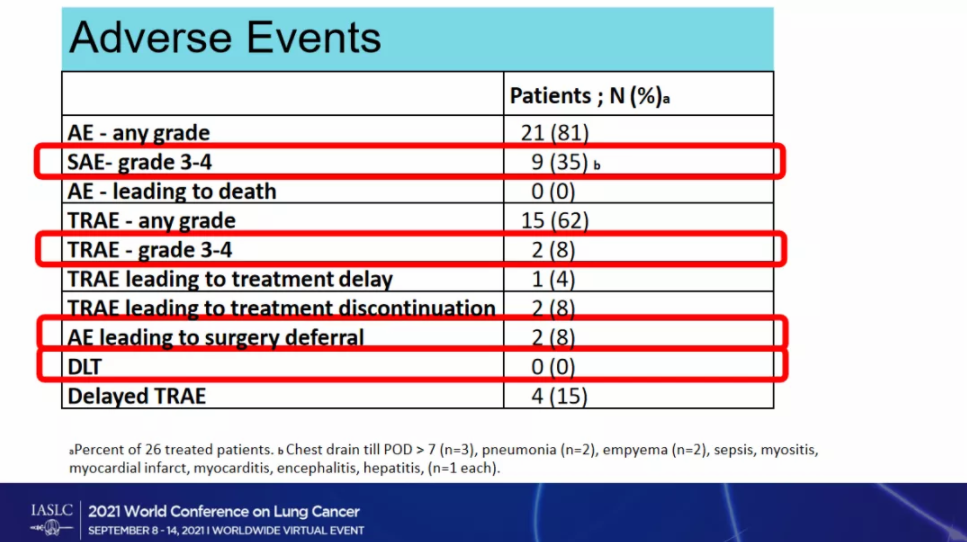
图1安全性数据
影像学肿瘤直径变化的中位数为-5%(范围,-43% 至 70%)。根据 RECIST评估标准,1例患者(4%;95% CI 0-11%)评估为部分缓解(PR),21 例患者(81%;95% CI 66-96%)评估为疾病稳定(SD),2例患者(8%;95% CI 0-18%)评估为疾病进展(PD),另有两例患者无法评估。
7 例患者(27%,95% CI 10-44%)达到 MPR,3 例(12%,95% CI 1-24%)达到完全病理学缓解(pCR)。MPR 患者的治疗-手术间隔较长。在中位随访 23个月 (95% CI 13-32) 时,26 例接受治疗的患者中有 2 例患者 (8%, 95% CI 0-18) 死亡,23 例手术患者中有1例(4%,95% CI 0-13%)出现疾病复发。
研究者表示:帕博利珠单抗用于早期 NSCLC 的新辅助治疗,MPR率为27%,pCR 率为12%,3-4 级TRAE率为8%。RP2D/S推荐以三周为间隔注射两剂帕博利珠单抗新辅助治疗,两周后进行手术,从治疗到手术的较长间隔与较高的 MPR 率相关。
湖南省肿瘤医院的杨农教授、张永昌教授团队设计了一项 II 期单臂试验,旨在探索特瑞普利单抗联合含铂双药化疗作为新辅助治疗初治潜在可切除NSCLC患者的抗肿瘤活性、安全性和可行性。研究结果在本次WCLC大会上公布,摘要号为P15.02。
本研究入组了具有组织学证实的潜在可切除 NSCLC (IIIA-IIIB)、无驱动基因突变的患者,所有患者在术前均接受了两个周期的特瑞普利单抗联合化疗,每 3 周一次。
在新辅助治疗结束后3-5周内进行术前影像学评估和手术指征评估。不能接受手术的患者将继续接受1-2 个周期的新辅助治疗后再进行评估,若此时无法达到手术标准则出组。术后30天内再给予 2 个周期的特瑞普利单抗 含铂双药辅助化疗,随后给予特瑞普利单抗单药巩固治疗13个周期。
研究结果显示:经过2-4个周期的新辅助治疗,15例患者(2个周期:12例;3-4个周期:3例)降期并达到手术标准。3例患者选择其他治疗(1例患者拒绝手术,2例患者不适合手术)。
18例患者的R0切除率为83.3%(15/18),在接受手术的15例患者中,8例患者 (8/15, 53.3%) 达到 MPR,其中 6 例患者 (6/15, 40.0%) 获得 pCR,未报告手术并发症。中位随访时间为 6 个月(范围:3-14),未出现复发或死亡。未观察到 3-4 级治疗TRAE,4 例患者 (4/15, 26.7%) 报告 1-2 级 TRAE。最常见的 TRAEs 是转氨酶升高,发生率为 20.0%。
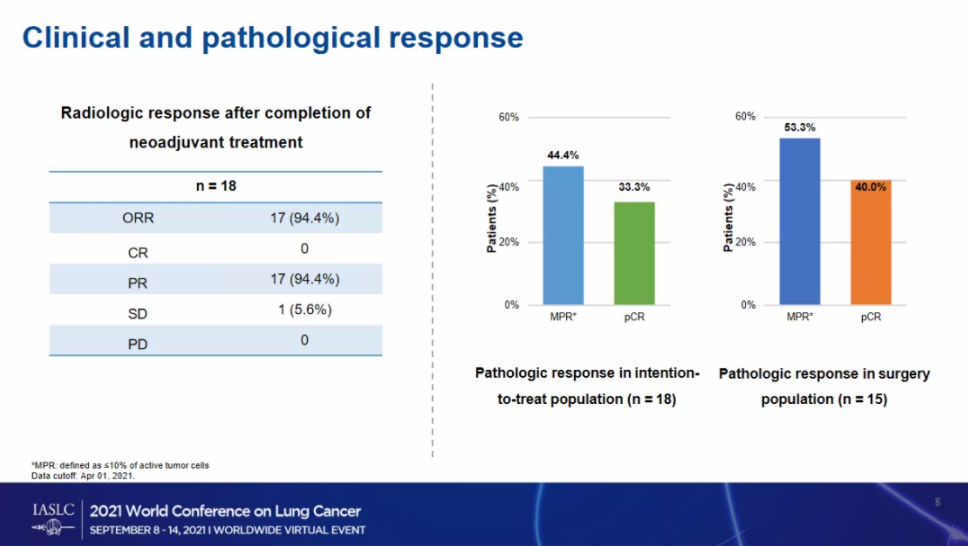
图2患者临床以及病理反应结果
该研究结果表明,特瑞普利单抗联合含铂双药化疗新辅助治疗潜在可切除NSCLC,显示出良好的临床疗效和耐受性。
NADIM研究是一项单臂II期试验,入组了46例可手术切除的IIIA期NSCLC患者,术前先接受纳武利尤单抗联合化疗新辅助治疗,术后再进行1年的纳武利尤单抗辅助治疗(240mg/2周,持续4个月;480mg/4周,持续8个月)。主要终点为意向治疗(ITT)人群和符合方案人群(PPP)的24个月PFS率。本次WCLC大会上,更新了NADIM研究的相关结果。
结果显示ITT人群在36个月和42个月时的PFS率均为69.6%(95%CI,54.1-80.7)。PP人群中36个月和42个月时的PFS 均为 81.1%(95%CI,64.4-90.5)。
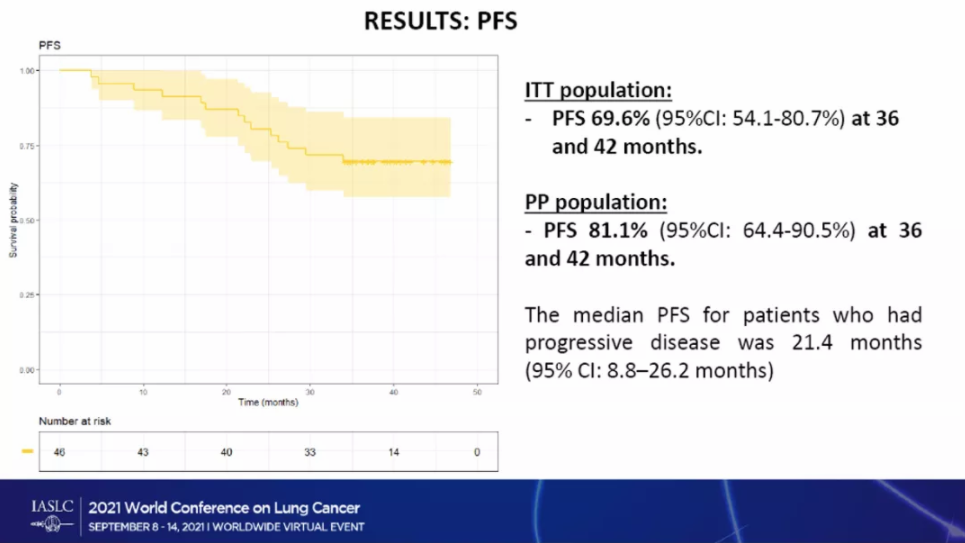
图3研究PFS结果
在mITT人群中,36个月和42个月时存活患者比例分别为81.86%(95% CI,66.8-90.6)和78.94%(95%CI,63.1-88.6)。同样,PP人群在36个月和42个月时的OS率分别为91.0%(95%CI,74.2-97.0)和87.3%(95%CI,69.3-95.1)。
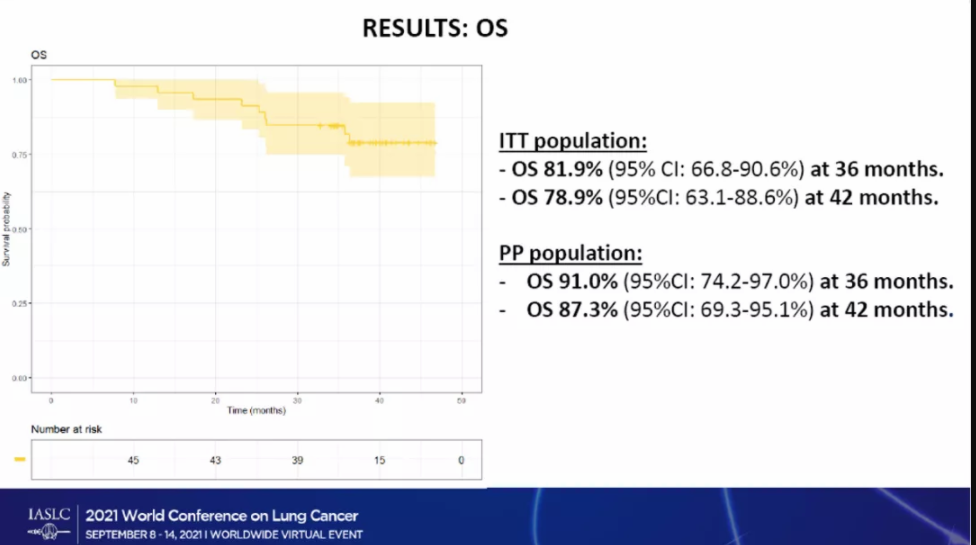
图4研究OS结果
探索性分析显示基于CT扫描和RECIST v1.1标准的临床反应并不能预测生存结果。然而,在多变量分析中,pCR或新辅助治疗后检测不到的循环肿瘤DNA(ctDNA)水平可以显著预测长期生存。
该研究是评估纳武利尤单抗联合标准化疗用于可切除IIIA期NSCLC患者新辅助治疗的首项临床研究。研究结果支持铂类化疗 纳武利尤单抗用于可切除IIIA期NSCLC患者的新辅助治疗。
印度肿瘤药房(India Pharmacy)是印度新德里肿瘤药房信息咨询服务平台,旨在为患者提供各类进口原研 进口仿制 最新研制等医药信息咨询 跨境医药电商直邮服务,让患者轻松获取全球最佳药品有更多选择,基本涵盖新特药 抗癌药 靶向药 丙肝 乙肝 高血压 糖尿病 痛风 等药品,欢迎咨询!官方微信 Yindu7689
