ASCO | 安进公布KRAS抑制剂最新结果
发布日期:2021-11-10 浏览次数:次

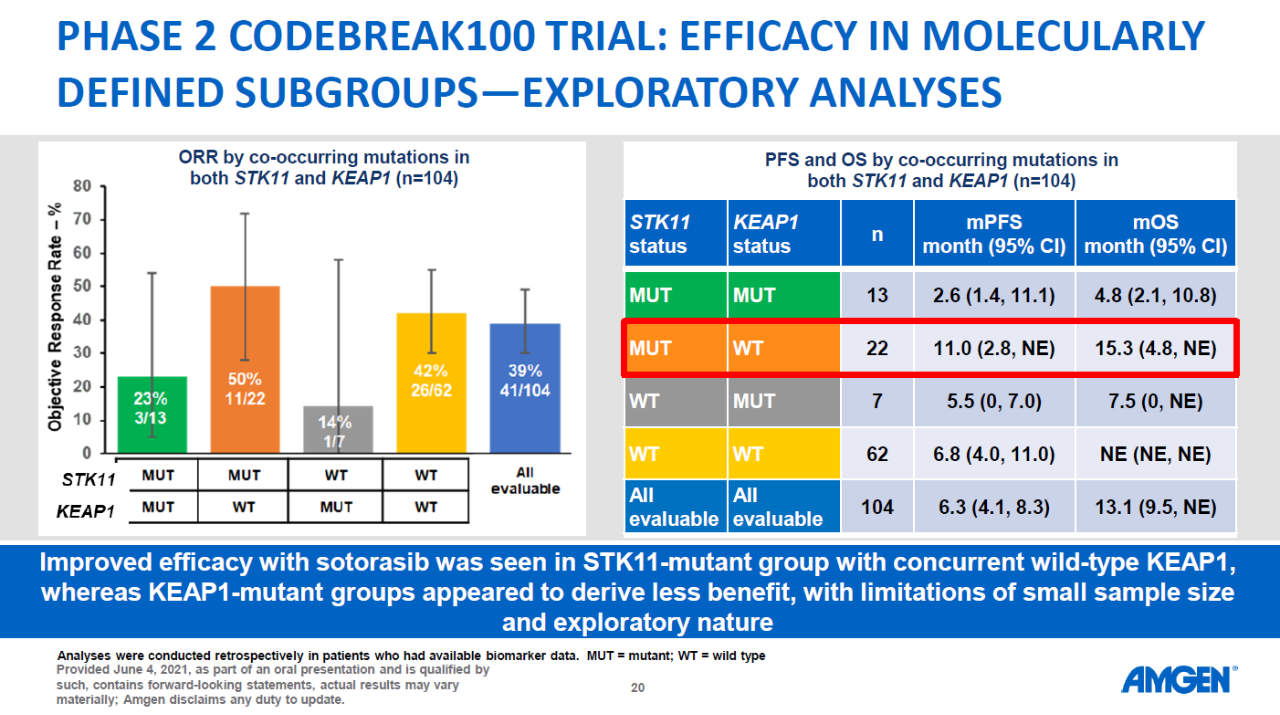
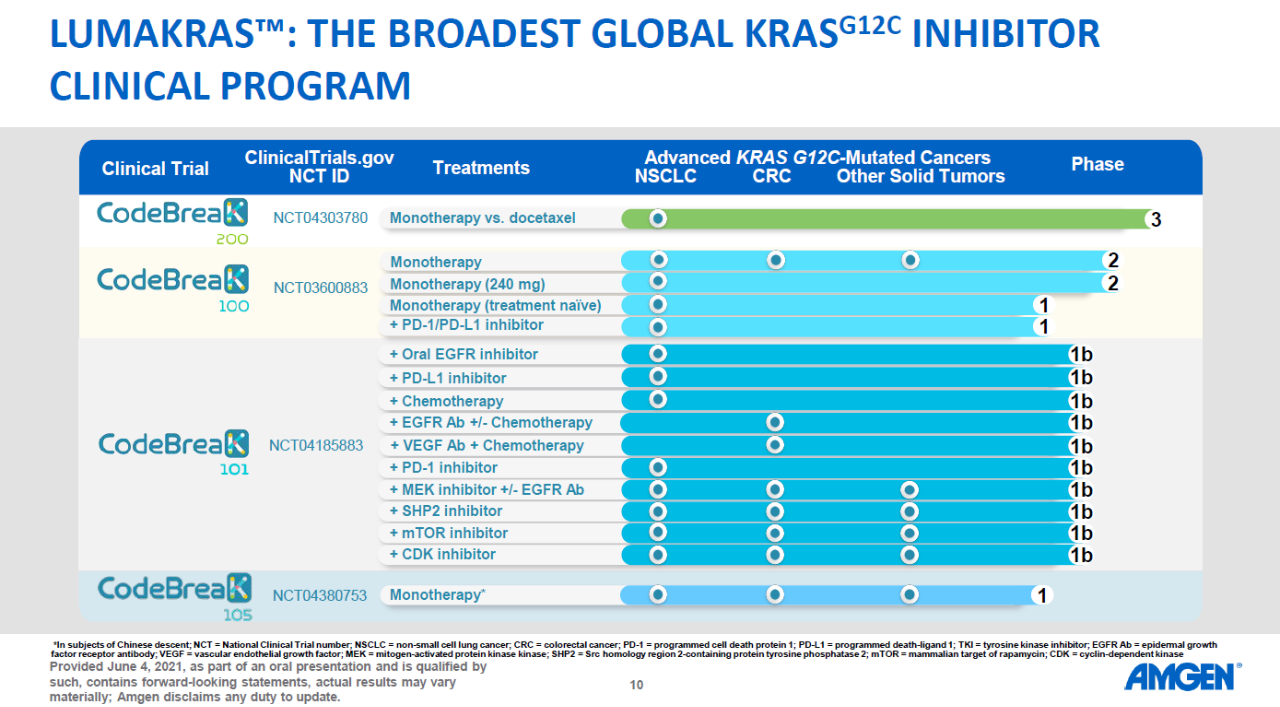
▲安进公司的Lumakras开发计划(图片来源:参考资料[2])
参考资料:
[1] Results From Phase 2 CodeBreaK 100 Show LUMAKRAS™ (sotorasib) Is The First And Only KRAS G12C Inhibitor With Overall Survival Data. Retrieved June 6, 2021, from https://www.amgen.com/newsroom/press-releases/2021/06/results-from-phase-2-codebreak-100-show-lumakras-sotorasib-is-the-first-and-only-kras-g12c-inhibitor-with-overall-survival-data
印度肿瘤药房(India Pharmacy)是印度新德里肿瘤药房信息咨询服务平台,旨在为患者提供各类进口原研 进口仿制 最新研制等医药信息咨询 跨境医药电商直邮服务,让患者轻松获取全球最佳药品有更多选择,基本涵盖新特药 抗癌药 靶向药 丙肝 乙肝 高血压 糖尿病 痛风 等药品,欢迎咨询!官方微信 Yindu7689
