肺癌丨精准医疗,KRAS突变靶向治疗新突破
发布日期:2022-08-27 浏览次数:次
KRAS它是在人体内发现的第一个癌基因。1982年,科学 家从人膀胱癌细胞系中克隆到了第一个癌基因,并很快确定这个癌基因是KRAS。但多年过去了, 科学家始终没有找到对付它的办法,于是给它冠以“不能开发药物的癌症靶点”的恶名 。KRAS突变是非小细胞肺癌一个重要的驱动基因,在西方人群中KRAS突变发生率达到20-30%,在亚洲人群这一发生率也达到7-10%。
doi: 10.1158/1078-0432.CCR-14-2148
中国肺腺癌中KRAS突变比例为8.3%,优势人群为男性、吸烟史、浸润性黏液型腺癌和实体型腺癌,G12C最常见(33.6%),G12D(23.9%)和G12V(22.1%)其次,见图2。
中国肺腺癌中KRAS突变亚型 DOI:10.2147/OTT.S96834
KRAS G12C
1. AMG510:II期,后线,ORR为37.10%、DCR为80.60%
2. MRTX849:Ⅰ/Ⅰb期和Ⅱ期,后线,ORR为45%、DCR为96%
KRAS 非G12C
3. VS-6766±defactinib:Ⅰ期,后线,肺癌有效率57%,卵巢癌有效率56%
4. VS-6766:Ⅰ期,后线,肺癌有效率30%,妇瘤60%
MAPK途径参与细胞的生长、发育、分化、凋亡等一系列细胞生理活动,是人类恶性肿瘤中最常见的致癌途径,与大约三分之一的实体瘤和一半多发性骨髓瘤相关。MAPK途径的经典通路之一就是RAS-RAF-MEK-ERK通路,目前临床上虽然已有了一些MAPK通路蛋白的抑制剂,但是考虑到它们对KRAS突变肿瘤的低效能和非肿瘤/非突变选择性疗法潜在的细胞毒性,靶向MAPK通路的疗法在KRAS突变肿瘤中仍是禁忌,所以亟需发展针对KRAS突变的具有肿瘤选择性的疗法。
AMG510是第一种直接靶向KRAS Gly12Cys的药物,并且已在KRAS Gly12Cys突变型非小细胞肺癌(NSCLC)中显示出抗肿瘤活性。在RAF突变型恶性肿瘤中,BRAF和MEK的联合抑制可改善BRAFV⁶⁰⁰(即Val600)突变型黑素瘤患者的总体生存率。总体而言,实体瘤RAS-RAF-MEK途径的靶向治疗,除了BRAFV⁶⁰⁰或KRAS Gly12Cys,其他仍未得到满足。
了解:RAS蛋白是一类鸟嘌呤核苷酸结合蛋白,具有GTP水解酶活性,当其与GDP结合时,处于非激活状态(关),而与GTP结合时被活化(开)。鸟嘌呤核苷酸转换因子(guanine nucleotide exchange factors,GEFs)促进GTP与RAS结合,继而激活多条信号通路,如RAF-MEK-ERK,P13K-AKT-mTOR 【PIK3信号通路通常能独立于RAF-MEK-ERK信号通路而促进肿瘤细胞生长。依赖于RAF-MEK-ERK信号存活的KRAS突变型肿瘤,被称为KRAS突变依赖型肿瘤,而部分肿瘤细胞可以通过其他信号通路继续生存,为KRAS突变非依赖型肿瘤】 和Ral-GDS等,调节肿瘤的生长、增殖、分化、和凋亡等生命过程。KRAS是RAS家族中最重要的基因,且KRAS突变是多种肿瘤中最常见的致癌因素之一。KRAS一旦发生突变,就会丧失GTP水解酶活性,进而持续活化,促使细胞持续增殖而癌变。
CodeBreak 100研究是一项I期、多中心、开放标签试验,研究纳入18岁以上组织学证实局部晚期或转移性实体瘤患者(对于NSCLC患者,要求既往接受过铂类联合治疗、靶向治疗或这两种治疗)且分子检测携带有KRAS p.G12C突变及ECOG评分0-2的患者。所有患者每天口服AMG 510(180、360、720和960 mg)一次,每个治疗周期为21天。主要终点是安全性,次要终点包括根据RECIST 1.1标准评估的ORR和DCR。
2020年ESMO年会上,安进公布了Sotorasib(AMG510)的I/II期试验初步数据;随后安进在顶级医学期刊NEJM杂志上公布了Sotorasib的完整I期试验结果。共计129例患者(包括59例NSCLC患者、42例结直肠癌患者和28例其他肿瘤患者)被纳入剂量递增和扩展队列。此项分析在接受了每日sotorasib单药治疗的全部1期试验人群中进行。中位随访时间为11.7个月(范围,4.6~21.2)。有107例患者(82.9%)停止治疗;最常见的停止治疗原因时疾病进展。截至数据截止日期2020年6月1日,有54例患者(41.9%)已死亡。中位治疗持续时间为3.9个月(范围,0~16.6)。共计74例患者(57.4%)接受了≥3个月治疗,38例患者(29.5%)接受了≥6个月治疗。
研究结果: NSCLC亚组的中位随访时间为11.7个月(范围,4.8-21.2)。 在59例NSCLC患者中,19例达到了经证实的部分缓解,33例达到了疾病稳定,中位无进展生存期为6.3个月; 因此, 32.2%的患者(95%置信区间[CI],20.62~45.64)达到了经证实的缓解,88.1%(95% CI,77.07~95.09)达到了疾病控制 (表3和图1A)。 在960 mg队列的34例患者中,35.3%(12例患者)达到了经证实的缓解,91.2%(31例患者)达到了疾病控制 。
本试验在所有剂量水平均观察到缓解。1例部分缓解患者接近完全缓解,其靶病变100%减少,但非靶病变持续存在(图1A)。NSCLC患者的CT图像见图1B。
表3:sotorasib对所有肿瘤类型的疗效

图1. 接受sotorasib治疗的NSCLC患者的肿瘤负荷相对于基线的变化
结直肠癌患者接受治疗后疗效一般,提示KRAS p.G12C可能并非结直肠癌的主要致癌驱动基因。
2020年WCLC年会,公布了II期CodeBreak 100研究结果。
研究结果:1 ) 截至2020年12月1日,中位随访时间为12.2个月。经评估,124例患者基线时至少有1个可测量病灶并可评估疗效。46例患者达到确认的缓解,其中3例为完全缓解,43例部分缓解。ORR为37.1%,DCR为80.6%,中位PFS为6.8个月。81%患者(101/124)观察到肿瘤缩小。中位DOR为10个月,数据分析截止时,43%(20/46)患者仍在接受治疗。
2)安全性:88例(69.8%)患者发生了任何级别的治疗相关不良事件(TRAE),并导致9例(7.1%)患者停药。26例(20.6%)发生≥3级TRAE,分别有6.3% (8/126)、5.6% (7/126)、4.0% (5/126)患者出现丙氨酸转氨酶升高、天门冬氨酸转氨酶升高和腹泻。

小结: 在既往接受过大量治疗,携带KRAS p.G12C突变的晚期实体瘤患者中,sotorasib表现出令人鼓舞的抗癌活性,对比二线标准化疗药多西他赛历史数据已经很优秀而安全性更好。
KRAS新药MRTX849初露峥嵘,疾病控制率高达96%
MRTX849是一款针对KRAS G12C突变开发的特异性小分子口服抑制剂[通过与处于失活状态的KRAS G12C突变体的不可逆结合,将它们“锁死”在失活构象,从而抑制KRAS介导的信号通路]。其对KRAS G12C突变体的抑制效果在纳摩尔(nM)水平即可显现,且具非常好的选择性,对KRAS G12C的选择性是野生型KRAS和其它蛋白上胱氨酸的1000倍以上。此外,MRTX849还具有口服利用度高、半衰期长等多个优点。
2020年10月,Mirati Therapeutics在第32届国际分子靶标与癌症治疗学研讨会(EORTC-NCI-AACR)上发表两项关于其KRAS G12C选择性抑制剂Adagrasib(MRTX849)的最新临床数据。Adagrasib在NSCLC队列,评估了51位患者(14位来自Ⅰ/Ⅰb期;37位来自Ⅱ期,虽然来自不同研究,但给药剂量相同),45%的患者具有客观反应(23/51位患者,其中5例患者的部分反应未经证实且仍在接受治疗),70%(16/23)的响应者肿瘤缩小40%以上,患者的疾病控制率为96%(49/51)。在中位随访时间3.6个月内,65%(33/51)的患者仍在接受治疗,83%(19/23)的反应者尚未进展,仍在接受治疗。
此外,Adagrasib(MRTX849)可以穿透血脑屏障,对于脑转移的患者也有效,会议上报道了一个患者案例:
一位77岁的女性KRAS G12C突变非小细胞肺癌患者,既往接受了多种方案的放化疗,PD-1治疗,仍然无法阻止病情进展,出现肝脏和脑部的多发转移,临床上已经没有更好的治疗方案,在接受试验性药物Adagrasib(MRTX849)治疗后7个周期后,不但肿瘤体积比基线减小67%,而且大脑中的转移瘤消失!目前仍在接受治疗。

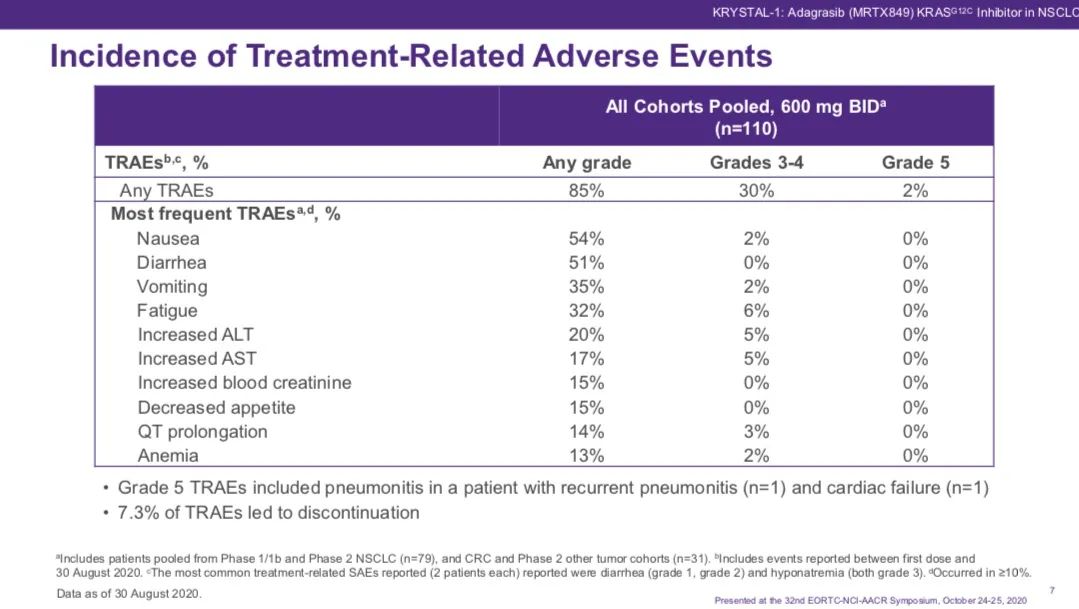
安全性: 在接受600mg BID的110名患者中,Adagrasib单药治疗的耐受性良好,任何级别的不良反应(TRAEs)发生率为85%,最常见(≥20%)不良反应为恶心(54%)、腹泻(51%)、呕吐(35%)、疲劳(32%)和ALT升高(20%),3级及以上不良反应发生比例为32%,分别发生1例复发性肺炎和心力衰竭的5级不良反应,4.5%的患者因治疗相关不良事件导致停药,不良反应导致停药的概率为7.5%。
1.FRAME研究[1]: 2020AACR年会上Verastam Oncology公司公布了其RAF/MEK抑制剂VS-6766,和特异性FAK抑制剂defactinib联用,治疗携带 RAS 突变的实体瘤患者的1期临床试验结果。 VS-6766是一款能够同时抑制RAF和MEK活性的小分子抑制剂 ,在临床前试验中,能够抑制多种RAS和RAF突变体介导的信号。而 defactinib能够特异性抑制FAK和相关蛋白激酶PYK2的活性 。两者联用,可能更全面地抑制癌细胞用来产生耐药性的信号通路。
研究中纳入的10例KRAS突变的非小细胞肺癌患者中有7例出现肿瘤缩小,其中1例G12V突变患者肿瘤缩小超过30%。该联合方案耐受性良好,最常见的不良反应是皮疹,肌酸激酶升高,天冬氨酸转氨酶升高,高胆红素血症和恶心,所有不良反应均可逆。二期临床研究推荐剂量:VS-6766每周两次(周一和周四),每次3.2mg,Defactinib每天二次,每次200mg,俩药每服用3周,停药1周。
2020年10月,Verastam Oncology公司公布的文件中披露了该研究进一步的临床研究数据。9例KRAS突变低级别浆液性卵巢癌患者,其中6例G12D,2例G12V,1例G12A,总有效率56%,其中2例已经缓解维持2.5年以上。 7例KRAS G12V突变非小细胞肺癌,VS-6766单药治疗4例,VS-6766联合Defactinib治疗2例,总有效率57% 。
相关研究发表柳叶刀[2]:这是一项单中心,开放标签的1期剂量递增和剂量扩展的篮子试验,研究共纳入58例18岁及以上的RAS–RAF–MEK途径突变的、晚期或转移性实体瘤或多发性骨髓瘤患者(包括51例实体瘤患者和7例多发性骨髓瘤患者)。至数据截止时的中位随访时间为2.3个月。
试验的剂量递增部分,在29例晚期或转移性实体瘤患者中,评估了三种间歇口服给药方案:以28天为一个周期,(1)每周3次4.0 mg或3.2 mg,(2)每周两次4.0 mg,(3)每周两次4.0 mg,但如果患者出现预先指定的毒性作用(2级或更严重的腹泻、皮疹或肌酐磷酸激酶升高),则减量为治疗3周、停药1周。
通过比较安全性,研究人员选择将每周两次4.0 mg作为2期试验的推荐剂量。该阶段观察到的剂量限制性毒性包括:接受每周3次4.0 mg的患者中,1例出现3级双侧视网膜色素上皮脱离;接受每周3次3.2 mg的患者中,2例出现3级皮疹,1例出现3级肌酐磷酸激酶升高。
接下来,在篮子剂量扩展阶段,针对29例携带RAS-RAF-MEK通路突变的晚期或转移性实体瘤和多发性骨髓瘤患者(包括12例非小细胞肺癌、5例妇科恶性肿瘤、4例结直肠癌、1例黑色素瘤和7例多发性骨髓瘤),评估了每周两次4.0mg的抗肿瘤毒性。
疗效: 1.在剂量扩展队列中 ,最终26例RAS/RAF突变的患者可以评价临床疗效,总体有效率为26%(7/26)。20例实体瘤患者的有效率为30%(6/20)。其中10例晚期非小肺癌患者中3例起效,有效率为30%,且这3例患者疗效均已超过6个月!其中,2例患者具有KRAS G12V突变,1例具有KRAS G12A突变。
2.在剂量递增队列中 ,其中5例妇瘤患者中,3例产生临床疗效,有效率为60%。其中1例是G12A突变的低级别浆液性卵巢癌患者,1例是BRAFV600E突变的低级别浆液性卵巢癌患者,这两例患者产生了非常持久的临床疗效。1例是G12V突变的子宫内膜癌患者。这三例患者均为铂类耐药。另外两例(G12A突变的透明细胞卵巢癌和G12V突变的宫颈癌)没有出现疗效。
3.在RAS / RAF突变的多发性骨髓瘤的7例患者中 ,有6例可评估。多发性骨髓瘤患者接受了严格的预处理,其中两名患者进行了自体干细胞移植。6名患者中有1名(16%(7%[95%CI 0.4–64.1])部分缓解,持续30周的无进展。接受过五线先前治疗的第二例患者在疾病稳定72周后仍继续接受治疗。
安全性: 结合两阶段数据来看,至少接受了一剂研究药物的患者中,治疗相关的最常见3-4级不良事件为皮疹(11例 [19%])、肌酐磷酸激酶升高(6例[11%])、低白蛋白血症(6例[11%])和疲劳(4例[7%]);5例(9%)患者出现治疗相关严重不良事件;没有与治疗相关的死亡;有8例患者(14%)在试验期间因疾病进展而死亡。
基于这些数据,研究人员认为,在携带RAS-RAF-MEK通路突变的多种癌症中,RAF/MEK抑制剂VS-6766的高度间歇性方案具有抗肿瘤活性,并且可耐受。
印度肿瘤药房(India Pharmacy)是印度新德里肿瘤药房信息咨询服务平台,旨在为患者提供各类进口原研 进口仿制 最新研制等医药信息咨询 跨境医药电商直邮服务,让患者轻松获取全球最佳药品有更多选择,基本涵盖新特药 抗癌药 靶向药 丙肝 乙肝 高血压 糖尿病 痛风 等药品,欢迎咨询!官方微信 Yindu7689
