帕纳替尼(Ponatinib)15mg
帕纳替尼(Ponatinib) 通用名称:Ponatinib 商品名称:iclusig 英文名称:Ponatinib 中文名称:帕纳替尼 全部名称:帕纳替尼、普纳替尼、iclusig、Ponatinib 适应症 帕纳替尼(Ponatinib)适用于治疗以下...


帕纳替尼(Ponatinib)
通用名称:Ponatinib
商品名称:iclusig
英文名称:Ponatinib
中文名称:帕纳替尼
全部名称:帕纳替尼、普纳替尼、iclusig、Ponatinib
适应症
帕纳替尼(Ponatinib)适用于治疗以下成人患者:
1、费城染色体阳性急性淋巴细胞白血病(Ph+ ALL)
1)新诊断的Ph+ ALL联合化疗。
基于诱导结束时的最小残留疾病(MRD)-阴性完全缓解(CR),在加速批准下批准此适应症。对该适应症的持续批准可能取决于在确认性试验中对临床益处的验证。
2)作为Ph+ ALL(未指示其他激酶抑制剂)或t 315i-阳性Ph+ ALL的单一疗法。
2、慢性粒细胞白血病(CML)
1)对至少两种既往激酶抑制剂耐药或不耐受的慢性期(CP) CML。
2)加速期(AP)或爆发期(BP) CML,不需要其他激酶抑制剂。
3)T315i-阳性CML(慢性期、加速期或爆发期)。
3、使用限制:对于新诊断出的CP-CML患者,不建议使用帕纳替尼(Ponatinib)进行治疗。
剂型和规格
帕纳替尼(Ponatinib)薄膜包衣片剂的规格为:
1、10毫克帕纳替尼(Ponatinib):椭圆形,白色至灰白色,双凸,一侧凹陷为“NZ”,另一侧平坦
2、15毫克帕纳替尼(Ponatinib):圆形、白色、双凸、一侧凹陷为“A5”,另一侧平坦
3、30毫克帕纳替尼(Ponatinib):圆形、白色、双凸、一侧凹陷为“C7”,另一侧平坦
4、45毫克帕纳替尼(Ponatinib):圆形、白色、双凸、一侧凹陷为“AP4”,另一侧平坦
用法用量
1、建议用量
1)新诊断Ph+ ALL
帕纳替尼(Ponatinib)联合化疗的推荐起始剂量为30毫克,口服,每日一次,在诱导结束时达到MRD-阴性(≤0.01% BCR::ABL1/ABL1) CR时,减少至15毫克口服,每日一次。继续帕纳替尼(Ponatinib)联合化疗20个周期,直至无反应或出现不可接受的毒性反应。
2)不需要其他激酶抑制剂或T315I阳性Ph+ ALL的Ph+ ALL单一疗法
尚未确定帕纳替尼(Ponatinib)的最佳剂量。
帕纳替尼(Ponatinib)的推荐起始剂量为45毫克,口服,每日一次。继续帕纳替尼(Ponatinib)直至无反应或出现不可接受的毒性。
如果3个月内仍无反应,则考虑停用帕纳替尼(Ponatinib)。
3)CP-CML
帕纳替尼(Ponatinib)的推荐起始剂量为45毫克口服,每日一次,当达到≤1% BCR::ABL1IS时,减少至15毫克口服,每日一次。失去反应的患者可以将帕纳替尼(Ponatinib)的剂量重新升至先前耐受的30毫克或45毫克口服剂量,每日一次。继续帕纳替尼(Ponatinib),直至在重新升高的剂量下无反应或出现不可接受的毒性。
如果3个月内仍未出现血液学应答,则考虑停用帕纳替尼(Ponatinib)。
4)AP-CML和BP-CML
尚未确定帕纳替尼(Ponatinib)的最佳剂量。
帕纳替尼(Ponatinib)的推荐起始剂量为45毫克,口服,每日一次。对于已实现主要细胞遗传学应答的加速期(AP) CML患者,考虑减少帕纳替尼(Ponatinib)的剂量。继续帕纳替尼(Ponatinib)直至无反应或出现不可接受的毒性。
如果3个月内仍无反应,则考虑停用帕纳替尼(Ponatinib)。
5)管理
告知患者以下事项:
a.帕纳替尼(Ponatinib)可与食物一起服用,也可不与食物一起服用。
b.整片吞下。请勿压碎、打碎、切割或咀嚼药片。
c.如果漏服了一剂药物,请在第二天的固定时间服用下一剂药物。
2、不良反应剂量调整
下表提供了针对不良反应的帕纳替尼(Ponatinib)建议修改剂量和针对不良反应的帕纳替尼(Ponatinib)建议减少剂量。
表:针对不良反应的帕纳替尼(Ponatinib)推荐剂量调整
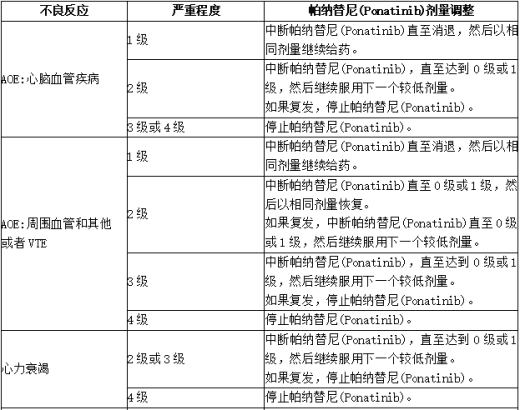
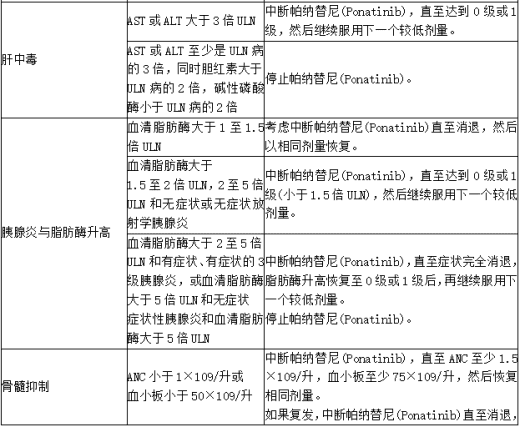
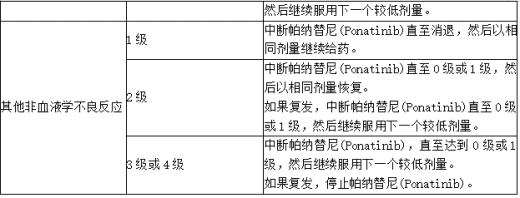
基于 CTCAE v5.0:1级轻度,2级中度,3级重度,4级危及生命
ULN =实验室正常值上限;AOE =动脉闭塞事件;VTE =静脉血栓栓塞事件;ANC =绝对中性粒细胞计数
表:帕纳替尼(Ponatinib)针对不良反应的推荐剂量减少量

3、强效CYP3A抑制剂联合用药的剂量调整
避免帕纳替尼(Ponatinib)与强效CYP3A抑制剂联合用药。如果不能避免合用一种强效CYP3A抑制剂,则按照下表中的建议减少帕纳替尼(Ponatinib)的剂量。停用强效CYP3A抑制剂3至5个消除半衰期后,恢复开始使用强效CYP3A抑制剂前耐受的帕纳替尼(Ponatinib)剂量。
表:与强效CYP3A抑制剂联合用药的推荐帕纳替尼(Ponatinib)剂量

4、肝功能损害患者的剂量
对于接受单药治疗的CP-CML、AP-CML、BP-CML和Ph+ ALL患者,对于既往有肝功能损害(Child-Pugh A、B或C)的患者,将帕纳替尼(Ponatinib)的起始剂量从每日一次45毫克口服降低至每日一次30毫克口服。
对于新诊断为Ph+ ALL的患者,当对轻度肝功能损害(Child-Pugh A)的患者给予帕纳替尼(Ponatinib)时,不建议调整剂量。密切监测中度或重度肝功能损害(Child-Pugh B或C)患者,并在出现不良反应时调整帕纳替尼(Ponatinib)剂量。
不良反应
1、动脉闭塞事件
2、静脉血栓栓塞事件
3、心力衰竭
4、肝毒性
5、高血压
6、胰腺炎
7、神经病
8、眼毒性
9、出血
10、液体滞留
11、心律失常
12、骨髓抑制
13、肿瘤溶解综合征
14、可逆性后部白质脑病综合征
15、伤口愈合不良和胃肠道穿孔
注意事项
1、动脉闭塞事件
动脉闭塞事件(AOE),包括死亡,发生在接受帕纳替尼(Ponatinib)治疗的患者中。
在PhALLCON中,163名患者中有6%发生了AOE,其中分别有3.1%、1.8%和1.2%的患者发生了心血管、脑血管和外周血管AOE。首次AOE发作的中位时间为11.3个月(范围:8天至2.8年)。3.7%的患者出现3级或4级AOEs最常见的3级或4级AOE为心肌梗死(1.2%)、外周动脉闭塞性疾病(1.2%)、心绞痛和脑血管意外(各0.6%)。1例(0.6%)患者发生致命性AOE猝死。AOE随着年龄的增长而更加频繁。
2、静脉血栓栓塞事件
接受帕纳替尼(Ponatinib)治疗的患者发生了严重或重度VTE。
在PhALLCON中,163例患者中有12%发生VTE,其中严重或重度(3级或4级)占3.1%。VTE包括深静脉血栓形成(6%)、浅静脉血栓形成(2.5%)、栓塞(1.8%)、肺栓塞和血栓形成(各1.2%)、颈静脉血栓形成和视网膜静脉阻塞(各0.6%)。首次VTE事件的中位发病时间为2.5个月(范围:6天至1.8年)。
在OPTIC中,起始剂量为 45 毫克的 94 名患者中,有 1 名患者发生了 VTE(1级视网膜静脉闭塞)。
在PACE中,449名患者中有6%发生VTE,其中严重或重度(3级或4级)占5.8%。VTE包括伴有视力丧失的深静脉血栓形成(2.2%)、肺栓塞(1.8%)、血栓性浅静脉炎(0.7%)、视网膜静脉阻塞(0.7%)和视网膜静脉血栓形成(0.4%)。62例BP-CML患者中10%、32例Ph+ ALL患者中9%、270例CP-CML患者中6%、85例AP-CML患者中3.5%发生VTE。
监测是否有室性心动过速的迹象。中断给药,然后根据复发/严重程度恢复相同或降低的剂量或中断帕纳替尼(Ponatinib)
3、心力衰竭
接受帕纳替尼(Ponatinib)治疗的患者中发生过致死性、严重或重度心力衰竭事件。
在PhALLCON中,163名患者中有6%发生心力衰竭;1.2%出现严重或重度(3级或4级)心力衰竭。最常报告的心力衰竭事件(> 1名患者)是脑钠肽(BNP)升高(2.5%)。
在OPTIC中,在接受45毫克起始剂量的94名患者中,13%的患者发生了心力衰竭;1.1%出现严重或重度(3级或4级)心力衰竭。最常报告的心力衰竭事件(>各1例)为左心室肥厚(3.2%)和BNP升高(3.2%)。
在PACE中,出现致命性或严重的心力衰竭。心力衰竭发生率为9%(449例);7%出现严重或重度(3级或以上)心力衰竭。最常报告的心力衰竭事件(≥2%)为充血性心力衰竭(3.1%)、射血分数下降(2.9%)和心力衰竭(2%)。
监测患者是否有与心力衰竭一致的体征或症状,并按照临床指示管理心力衰竭。中断给药,然后以减少的剂量恢复给药,或因新的或恶化的心力衰竭而中断帕纳替尼(Ponatinib)。
4、肝中毒
帕纳替尼(Ponatinib)可导致肝中毒,包括肝衰竭和死亡。3例患者发生了导致死亡的严重肝功能衰竭,其中1例患者的肝功能衰竭发生在开始接受帕纳替尼(Ponatinib)治疗后1周内。这些死亡病例发生在接受单药治疗的BP-CML或Ph+ ALL患者中。
在PhALLCON中,163名患者中有66%发生肝毒性;30%出现3级或4级肝毒性。肝毒性发生的中位时间为15天(范围:1天至10个月)。最常见的肝毒性事件是丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)、γ-谷氨酰转移酶(GGT)、胆红素和碱性磷酸酶升高,白蛋白减少,血纤维蛋白原减少。在报告ALT或AST升高的73名患者中,有6%的患者在最后一次随访时仍未消退。
在OPTIC中,在开始服用45毫克剂量的94名患者中,28%的患者发生了肝毒性;6%出现3级或4级肝毒性。肝毒性发生的中位时间为1.9个月,范围为3天至4.1年。最常见的肝毒性事件是ALT、AST、碱性磷酸酶和GGT升高。在报告ALT或AST升高的21名患者中,有29%的患者在最后一次随访时事件尚未解决。
在PACE中,449名患者中有32%发生肝毒性;13%经历过3级或4级肝毒性。肝毒性发生的中位时间为3.1个月,范围为1天至4.9年。最常见的肝毒性事件是ALT、AST、GGT、胆红素和碱性磷酸酶升高。在报告ALT或AST升高的88名患者中,有9%的患者在最后一次随访时事件尚未解决。
在基线时监测肝功能检测,然后至少每月一次或根据临床指示进行监测。中断给药,然后根据复发/严重程度恢复低剂量给药或中断帕纳替尼(Ponatinib)。
5、高血压
接受帕纳替尼(Ponatinib)治疗的患者出现了严重或重度高血压,包括高血压危象。
在PhALLCON中,163名患者中有34%发生高血压;14%发生严重或重度高血压。根据生命体征数据,60例初始血压正常的患者中有15例(25%)出现1级血压升高,134例初始血压低于2级的患者中有67例(50%)出现2级血压升高,63例出现3级血压升高,初始血压低于3级的患者160例(39%)。
在OPTIC中,在开始服用45毫克剂量的94名患者中,32%的患者报告有高血压事件;12%发生严重或重度高血压。根据生命体征数据,18例初始血压正常的患者中有8例(44%)出现1级血压升高,81例初始血压低于2级的患者中有28例(35%)出现2级血压升高,92例初始血压低于3级的患者中有18例(20%)出现3级血压升高。3例(3.2%)出现高血压危象。
在PACE中,449名患者中有32%报告有高血压事件;13%发生严重或重度高血压。在基线血压正常的患者中,449名患者中有44%出现2级或更高的收缩压或舒张压基线后升高。1级BP升高发生率为26%,2级为45%,3级为26%。两名患者(< 1%)出现4级高血压(高血压危象)。
患者可能需要对伴有意识模糊、头痛、胸痛或气促的高血压进行紧急临床干预。根据基线和临床指示监测血压,并根据临床指示管理高血压。如果未对高血压进行药物控制,则中断、减少剂量或停止帕纳替尼(Ponatinib)。对于显著恶化、不稳定或治疗耐药的高血压,中断帕纳替尼(Ponatinib)并考虑评估肾动脉狭窄。
6、胰腺炎
接受帕纳替尼(Ponatinib)治疗的患者发生了严重或重度胰腺炎。
在PhALLCON中,163例患者中有34%发生胰腺炎;15%出现严重或重度(3级或4级)胰腺炎。胰腺炎发病的中位时间为8天(范围:1天至2年)。在7例导致剂量调整的临床胰腺炎患者中,胰腺炎三周内消退。25%的患者出现淀粉酶升高的实验室检测异常,而60%的患者出现脂肪酶升高。
在OPTIC中,在开始接受45毫克剂量治疗的94名患者中,23%的患者发生胰腺炎;15%出现严重或重度(3级或4级)胰腺炎。胰腺炎导致1.1%的患者停药,20%的患者停药和/或减少剂量。胰腺炎发病的中位时间为23天(范围:3天至5.6个月)。在2例导致剂量调整或治疗中止的临床胰腺炎患者中,胰腺炎在2周内消退。11%的患者出现淀粉酶升高的实验室检测异常,34%的患者出现脂肪酶升高。
在PACE中,449名患者中有26%发生胰腺炎;17%出现严重或重度(3级或4级)胰腺炎。胰腺炎导致0.4%的患者停药,17%的患者停药和/或减少剂量。胰腺炎发病的中位时间为29天(范围:1天至4年)。在28例导致剂量调整或治疗中止的临床胰腺炎病例中,有19例在2周内消退。18%的患者出现淀粉酶升高的实验室检测异常,而39%的患者出现脂肪酶升高。
前2个月每2周监测一次血清脂肪酶,此后每月或根据临床指示监测一次。考虑对有胰腺炎或酒精滥用史的患者进行额外的血清脂肪酶监测。中断给药,然后根据严重程度恢复相同或减少的剂量或中断帕纳替尼(Ponatinib)。当脂肪酶升高伴有腹部症状时,评估胰腺炎。
7、新诊断慢性期CML的毒性增加
在一项对新诊断的CP-CML患者进行一线治疗的前瞻性随机临床试验中,单剂帕纳替尼(Ponatinib)45毫克每日一次增加了严重不良反应的风险。与单剂伊马替尼400毫克每日一次相比增加2倍。治疗的中位暴露时间小于6个月。为了安全起见,试验暂停了。与伊马替尼组相比,帕纳替尼(Ponatinib)组发生动脉和静脉血栓形成和闭塞的频率至少高一倍。与接受伊马替尼治疗的患者相比,接受帕纳替尼(Ponatinib)治疗的患者出现骨髓抑制、胰腺炎、肝毒性、心力衰竭、高血压以及皮肤和皮下组织疾病的发生率更高。I结论对于新诊断出的CP-CML患者,不建议使用或不使用ICG进行治疗。
8、神经病
在PhALLCON中,163名患者中有68%发生周围神经病变;3.1%出现3级或4级周围神经病变。最常见的周围神经病为周围神经病(33%)、感觉异常(22%)和周围感觉神经病(12%)。周围神经病变的中位发病时间为1.1个月(范围:1天至17.2个月)。163例患者中有0.6%报告有颅神经病。
在OPTIC中,在开始接受45 mg剂量治疗的94名患者中,9%的患者发生了神经病。6%的患者发生周围神经病变。最常报告的周围神经病为感觉减退(2.1%)、肌无力(2.1%)和感觉异常(2.1%)。2例患者出现颅神经病。周围神经病变和颅神经病变的中位发病时间为7.7个月(范围:1.5个月至1.4年)和2.1年(范围:第1天至4.2年)。
在PACE中,22%的患者发生神经病;2.4%出现3级或4级神经病变。449例患者中有20%发生周围神经病变;1.8%出现3级或4级周围神经病变。最常见的周围神经病为感觉异常(5%)、周围神经病(4.5%)和感觉减退(3.6%)。3%的患者出现颅神经病;0.7%为3级或4级。周围神经病变和颅神经病变的中位发病时间为5.3个月(范围:1天至4.6年)和1.2年(范围:18天至4年)。
监测患者的神经病变症状,如感觉减退、感觉亢进、感觉异常、不适、灼热感、神经性疼痛或无力。中断给药,然后根据复发/严重程度恢复相同或减少的剂量或中断帕纳替尼(Ponatinib)。
9、眼毒性
在帕纳替尼(Ponatinib)治疗的患者中发生了导致失明或视力模糊的严重眼毒性。
在PhALLCON中,163名患者中有33%发生眼毒性;1.8%出现严重或重度眼毒性。最常见的眼部毒性反应为视力模糊和干眼。4.3%的患者出现视网膜毒性;0.6%出现3级视网膜静脉阻塞。最常见的视网膜毒性事件(> 1名患者)为视网膜出血(1.8%)。
在OPTIC中,在接受45毫克起始剂量的94名患者中,11%的患者发生眼毒性;1.1%出现严重或重度眼毒性。最常见的眼部毒性反应为视力模糊和眼部疼痛。2.1%的患者出现视网膜毒性,包括年龄相关性黄斑变性和视网膜静脉阻塞。
在PACE中,449名患者中有30%发生眼毒性;3.6%出现严重或重度眼毒性。最常见的眼部毒性反应为干眼、视力模糊和眼部疼痛。3.6%的患者出现视网膜毒性。最常见的视网膜毒性反应为黄斑水肿、视网膜静脉阻塞、视网膜出血和玻璃体漂浮物(各0.7%)。
在基线和治疗期间定期进行全面的眼部检查。
10、出血
接受帕纳替尼(Ponatinib)治疗的患者中发生了致命性和严重的出血事件。
在PhALLCON中,163例患者中有31%发生出血;2.5%出现严重出血。颅内出血是最常报告的严重出血,发生率为1.2%。
在OPTIC中,在开始接受45毫克剂量治疗的94名患者中,12%的患者发生出血;1例出现严重硬膜下血肿。
在PACE中,449名患者中有28%发生出血;6%发生严重出血,1.3%发生致命性出血。在AP-CML、BP-CML和Ph+ ALL患者中,严重出血事件的发生率较高。胃肠道出血和硬膜下血肿是最常报告的严重出血,各发生在0.9%的患者中。大多数出血发生在4级血小板减少症患者。
监测出血情况,并按照临床指示管理患者。中断给药,然后根据复发/严重程度恢复相同或减少的剂量或中断帕纳替尼(Ponatinib)。
11、液体潴留
接受帕纳替尼(Ponatinib)治疗的患者中发生了致命和严重的液体潴留事件。
在PhALLCON中,163名患者中有24%出现液体潴留;1.2%出现严重积液,包括心包积液(1.2%)。最常见的积液为外周水肿(11%)和胸腔积液(6%)。
在OPTIC中,在开始接受45 mg剂量治疗的94名患者中,5%的患者出现液体潴留。最常见的液体潴留事件为外周水肿(2.1%)和胸腔积液(2.1%)。
在PACE中,449名患者中有33%发生液体潴留事件;4.5%出现严重积液。一例脑水肿是致命的。严重积液包括胸腔积液(1.6%)、心包积液(1.6%)和血管性水肿(0.4%)。最常见的液体潴留事件为外周水肿(17%)、胸腔积液(9%)、心包积液(4.2%)和外周肿胀(3.8%)。
监测液体潴留,并按照临床指示管理患者。中断给药,然后根据复发/严重程度恢复相同或减少的剂量或中断帕纳替尼(Ponatinib)。
12、心律失常
在PhALLCON中,163名患者中有22%发生心律失常事件;2.5%发生3级或4级心律失常,包括心动过速、晕厥、房颤和室上性心动过速(各0.6%)。
在OPTIC中,在开始接受45毫克剂量治疗的94名患者中,16%的患者发生了心律失常;4.3%发生3级或4级心律失常。3级或4级心律失常包括房颤、心肺骤停、室上性期外收缩和晕厥。
在PACE中,449名患者中有20%发生心律失常;7%发生3级或4级心律失常。在报告有心律失常的89名患者中,3.4%的患者发生了室性心律失常,其中一起事件为3级或4级。1%的患者出现导致起搏器植入的症状性缓慢心律失常。房颤是最常见的心律失常(8%),3.3%为3级或4级。其他3级或4级心律失常事件包括晕厥(2%)、心动过速和心动过缓(各0.4%)、QT间期延长、心房扑动、窦性心动过缓、室上性心动过速、室性心动过速、房性心动过速、房室传导阻滞完全、心肺骤停、意识丧失和窦房结功能障碍(各0.2%)。31例患者因心律失常住院。
监测提示心率减慢(晕厥、头晕)或心率加快(胸痛、心悸或头晕)的体征和症状,并按照临床指示对患者进行管理。中断给药,然后根据复发/严重程度恢复相同或减少的剂量或中止帕纳替尼(Ponatinib)。
13、骨髓抑制
在PhALLCON中,163例患者中有66例发生中性粒细胞减少(63例发生3级或4级),65例发生血小板减少(62例发生3级或4级),53例发生贫血(38例发生3级或4级)。出现3级或4级骨髓抑制的中位时间为27天(范围:1天至9.2个月)。
在OPTIC中,接受45毫克起始剂量治疗的94例患者中,55%发生中性粒细胞减少(22例发生3级或4级),65%发生血小板减少(31例发生3级或4级),35%发生贫血(14例发生3级或4级)。出现3级或4级骨髓抑制的中位时间为1.4个月(范围:1天至1.2年)。
在PACE中,中性粒细胞减少发生率为56%(3级或4级发生率为34%),血小板减少发生率为63%(3级或4级发生率为40%),贫血发生率为52%(3级或4级发生率为20%)。AP-CML患者的骨髓抑制发生率较高,
BP-CML和Ph+ ALL高于CP-CML患者。治疗早期观察到严重骨髓抑制(3级或4级),中位发病时间为29天(范围:1天至4.1年)。
在前3个月每2周获取一次全血细胞计数,然后每月或根据临床指示获取一次。如果ANC小于1 x 109/L或血小板小于50 x 109/L,则中断ICLUSIG,直至ANC至少为1.5 x 109/L,血小板至少为75 x 109/L,然后以相同或减少的剂量恢复。
14、肿瘤溶解综合征
在PhALLCON中,163名患者中有0.6%出现严重肿瘤溶解综合征(TLS)。10%的患者发生高尿酸血症。
在OPTIC中,在开始接受45毫克剂量治疗的94名患者中,1.1%的患者发生了严重的TLS。2.1%的患者发生高尿酸血症。
在PACE中,449名患者中有0.4%出现严重TLS。1例发生在晚期AP-CML患者中,1例发生在BP-CML患者中。7%的患者发生高尿酸血症。
开始帕纳替尼(Ponatinib)前,确保充分水化并治疗高尿酸血症。
15、可逆性后部白质脑病综合征
可逆性后部白质脑病综合征(RPLS;也称为可逆性后部脑病综合征)的研究。患者可表现为高血压、癫痫、头痛、警觉性下降、精神功能改变、视力丧失以及其他视觉和神经障碍。必须进行磁共振成像(MRI)以确认诊断。中断帕纳替尼(Ponatinib)直至问题解决。RPLS病消退后,患者恢复帕纳替尼(Ponatinib)的安全性尚不清楚。
16、伤口愈合不良和胃肠道穿孔
接受帕纳替尼(Ponatinib)治疗的患者出现伤口愈合受损。择期手术前至少1周。在大手术后至少2周内不要给药,直到伤口充分愈合。在伤口愈合并发症解决后恢复帕纳替尼(Ponatinib)的安全性尚未确定。
17、胚胎-胎儿毒性
根据其作用机制和动物研究发现,帕纳替尼(Ponatinib)对孕妇给药时可能会对胎儿造成伤害。在动物生殖研究中,在器官形成期间对妊娠动物口服帕纳替尼(Ponatinib),在低于45毫克/天最大推荐人用剂量的暴露量下引起不良发育影响。告知孕妇对胎儿的潜在风险。告知有生殖潜力的雌性在使用帕纳替尼(Ponatinib)治疗期间和最后一次给药后3周内使用有效避孕方法。
特殊人群用药
1、妊娠期
基于在动物中的发现及其作用机制,帕纳替尼(Ponatinib)对孕妇给药时会对胎儿造成伤害。尚无关于孕妇使用帕纳替尼(Ponatinib)的可用数据。在动物生殖研究中,在器官形成期间对妊娠动物口服帕那替尼,在低于45毫克/天最大推荐人用剂量的剂量下引起了不良发育影响。告知孕妇对胎儿的潜在风险。
2、哺乳期
前尚无关于帕纳替尼(Ponatinib)在人乳中的存在、对母乳喂养儿童的影响或对产奶量的数据。由于母乳喂养的儿童可能出现严重的不良反应,建议女性在使用帕纳替尼(Ponatinib)治疗期间和最后一次给药后1周内不要进行母乳喂养。
3、具有生殖潜力的男性和女性
妊娠期女性服用帕纳替尼(Ponatinib)可能对胎儿造成伤害。
在开始使用帕纳替尼(Ponatinib)之前,检查具有生殖潜力的女性的妊娠状态。
告知有生殖潜力的女性在使用帕纳替尼(Ponatinib)治疗期间和最后一次给药后3周内使用有效避孕方法。
根据动物数据,帕纳替尼(Ponatinib)可能会损害具有生殖潜力的MV性的生育力。尚不清楚这些对生育力的影响是否可逆。
4、儿童使用
帕纳替尼(Ponatinib)在儿童患者中的安全性和有效性尚未确定。
5、老年用药
在163例在PhALLCON中接受帕纳替尼(Ponatinib)治疗的Ph+ALL患者中,21%为65岁及以上,7%为75岁及以上。总体而言,与较年轻患者相比,未观察到65岁及以上患者之间帕纳替尼(Ponatinib)疗效的差异。65岁及以上的患者中有21% (7/34)发生AOE,65岁以下的患者中有2.3% (3/129)发生AOE。
在开始服用45毫克视神经管帕纳替尼(Ponatinib)的94例CP-CML患者中,17%为65岁及以上,2.1%为75岁及以上。与65岁以下的患者(47%)相比,65岁及以上的患者在12个月时的BCR::ABL1IS率较低(27%)。65岁及以上的患者中有38% (6/16)发生AOE,65岁以下的患者中有9% (7/78)发生AOEs。
在449例在PACE中接受帕纳替尼(Ponatinib)治疗的患者中,35%为65岁及以上,8%为75岁及以上。在CP-CML患者中,65岁及以上患者的主要细胞遗传学应答率(40%)低于65岁以下患者(65%)。
65岁及以上的患者更可能出现不良反应,包括血管闭塞、血小板计数下降、外周水肿、脂肪酶增加、呼吸困难、乏力、肌肉痉挛和食欲下降。一般而言,老年患者的剂量选择应谨慎,这反映了肝功能、肾功能或心功能下降以及伴随疾病或其他药物治疗的频率更高。
6、肝功能损害
与肝功能正常的患者相比,肝功能损害的患者更可能发生不良反应。对于接受单药治疗的CP-CML、AP-CML、BP-CML和Ph+ ALL患者,对于已有肝功能损害的患者(Child-Pugh A、B或C),应减少帕纳替尼(Ponatinib)的起始剂量。对于新诊断为Ph+ ALL的患者,当对轻度肝功能损害(Child- Pugh A)的患者给予帕纳替尼(Ponatinib)时,不建议调整剂量。没有新诊断为Ph+ ALL且先前存在中度或重度肝功能损害(Child-Pugh B或C)的患者的临床数据,应密切监测患者的不良反应发生率是否可能增加。在出现不良反应时修改帕纳替尼(Ponatinib)剂量。尚未在肝功能损害患者中研究多剂量或高于30毫克剂量的安全性。
药物相互作用
其他药物对帕纳替尼(Ponatinib)的影响
1、强效CYP3A抑制剂
帕纳替尼(Ponatinib)与一种强效CYP3A抑制剂联合用药会增加波那替尼的血浆浓度,这可能会增加帕纳替尼(Ponatinib)不良反应的风险。避免帕纳替尼(Ponatinib)与强效CYP3A抑制剂联合用药。如果无法避免帕纳替尼(Ponatinib)与强效CYP3A抑制剂联合给药,则应减少帕纳替尼(Ponatinib)的剂量。
2、强CYP3A诱导剂
帕纳替尼(Ponatinib)与强效CYP3A诱导剂联合给药会降低波那替尼的血浆浓度。避免将帕纳替尼(Ponatinib)与强效CYP3A诱导剂联合用药,除非益处大于降低帕那替尼暴露的风险。监测患者是否出现疗效降低的情况。建议选择无CYP3A诱导可能性或CYP3A诱导可能性极小的合用药物。
药物过量
临床试验中曾报告过帕纳替尼(Ponatinib)用药过量。据估计,一名患者经鼻胃管服用了540毫克。过量用药后2小时,患者的未校正QT间隔时间为520ms。随后的心电图显示窦性心律正常,未校正QT间隔时间为480ms和400ms。患者在过量用药后9天死于肺炎和脓毒症。另一名患者在第1周期第2天自行服用165毫克。患者在第3天出现疲劳和非心脏性胸痛。在患者中,每日90毫克多次给药持续12天,导致肺炎、全身炎性反应、房颤和中度心包积液。
如果用药过量,停止帕纳替尼(Ponatinib)观察患者并提供适当的支持性治疗。
成分
活性成分:Ponatinib
非活性成分:一水乳糖、微晶纤维素、淀粉羟乙酸钠(B型)、胶体二氧化硅和硬脂酸镁。
片剂包衣:滑石粉、聚乙二醇、聚乙烯醇和二氧化钛。
性状
片剂
贮存方法
1、将帕纳替尼(Ponatinib)储存在20°C至25°C的室温下。
2、将帕纳替尼(Ponatinib)和所有药物放在儿童拿不到的地方。。
生产厂家
武田制药
立即咨询
